
代谢物同型半胱氨酸(Hcy)作为一项重要的人体健康指标,其水平升高被作为卒中等心脑血管病的危险因素;同时Hcy也调控心脏等组织器官发育过程,临床及模式动物研究提示Hcy是包括先天性心脏病(CHD)、神经管畸形(NTD)、唐氏综合征(DS)在内的出生缺陷的独立风险因子,但致病机理不明。
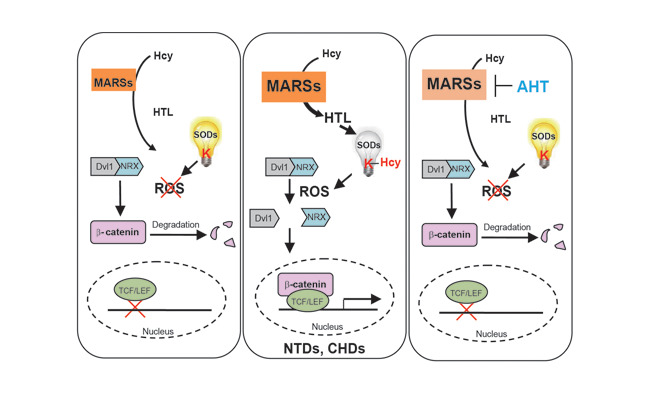
赵世民教授团队等发现:同型半胱氨酸可以修饰蛋白质赖氨酸残基影响修饰底物蛋白性质,抑制修饰酶甲硫氨酰tRNA合成酶(MARS)的活性可显著降低神经管畸形和先天性心脏病这两种高Hcy相关出生缺陷的发生率。甲硫氨酰tRNA合成酶MARS将Hcy信号以蛋白质赖氨酸Hcy修饰的形式传递至下游底物蛋白;进一步通过蛋白质学、生物信息学的方法鉴定到包括超氧化物歧化酶(SOD1/2)在内的数百种蛋白质赖氨酸Hcy修饰底物蛋白;并且高Hcy信号通过蛋白质赖氨酸Hcy修饰抑制SOD1/2活性,导致细胞内ROS累积进而调控凋亡及Wnt信号通路;进而参与神经管畸形和先天性心脏病的发生。
上述发现为血液Hcy水平升高是已知的先天性心脏病等多种出生缺陷的重要风险因素,但在细胞及动物水平抑制同型半胱氨酸水平均不能降低这些疾病的发病率提供了新解释,因为高Hcy通过MARS致病。重要的是,他们用Hcy结构类似的小分子化合物乙酰同型半胱氨酸硫醚(AHT)竞争抑制 Hcy修饰,在小鼠模型中显著降低了神经管畸形和先天性心脏病这两种高Hcy相关出生缺陷的发生率,为临床干预提供了新的方向。
这一成果于2020年1月31日发表于EMBO Molecular Medicine杂志。复旦大学生物医学研究院徐薇副研究员,附属妇产科医院/代谢与整合生物学研究院赵世民教授、王红艳教授,生命科学学院赵健元教授团队参与了研究,梅馨予博士等人为同等贡献第一作者。
论文链接:




 复旦大学网上办事服务大厅
复旦大学网上办事服务大厅 复旦大学实验室安全教育与管理平台
复旦大学实验室安全教育与管理平台