
脂肪酸是机体的基本营养物质之一,参与了能量储存和生物膜合成等多种重要的生命进程。由于脂肪酸具有很强的疏水性,并且缺少好的标记方法,因此脂肪酸的转运机制并不清楚。目前普遍接受的观点认为,餐后小肠主要以被动扩散的形式吸收脂肪酸,而在其它代谢器官中则主要依赖于蛋白辅助的脂肪酸吸收。但是,脂肪酸如何跨过细胞膜并进入到细胞内目前并不清楚。
在已知的脂肪酸转运蛋白中,CD36是研究相对较多的一个,在脂肪酸的吸收中扮演着重要的角色[1]。CD36分子上具有一个脂肪酸结合位点,小鼠脂肪和肌肉组织大约50%的脂肪酸吸收是由CD36贡献的[2]。在脂肪细胞中,CD36主要位于细胞膜上的caveolae结构中,并且其脂肪酸吸收活性依赖于caveolae结构[3]。
复旦大学代谢与整合生物学研究院赵同金课题组于2019年在Cell Reports发表的论文中发现两个棕榈酰基转移酶(palmitoyl acyltransferase,因其结构含有保守的DHHC motif,也被称为DHHCs)DHHC4和DHHC5分别在高尔基体和细胞质膜上对CD36进行棕榈酰化修饰,从而维持CD36的质膜定位并促进其脂肪酸吸收的活性(图1)[4]。
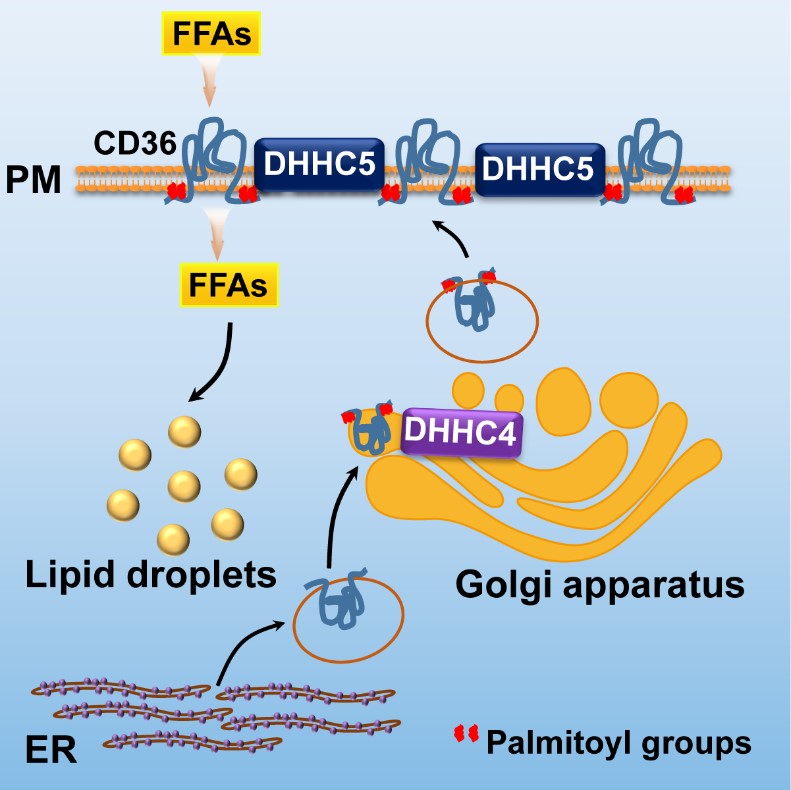
图1 DHHC4和DHHC5通过棕榈酰化修饰CD36调控脂肪酸吸收
此基础上,赵同金课题组与陈帅课题组合作进一步研究了CD36促进脂肪酸吸收的方式,并于9月21日在Nature Communications发表题为CD36 facilitates fatty acid uptake by dynamic palmitoylation-regulated endocytosis的研究论文(图2)。研究证明CD36能够以内吞的方式吸收脂肪酸,并且发现CD36的动态棕榈酰化在这一过程中扮演着不可或缺的角色。研究发现长链脂肪酸能够促进CD36从脂肪细胞的细胞膜上进行内吞,并且证明CD36以内吞的方式进行脂肪酸的吸收。
进一步的研究发现,CD36的动态棕榈酰化在其内吞脂肪酸的过程中发挥着不可或缺的作用:CD36需要发生棕榈酰化修饰才能定位在细胞质膜上以结合脂肪酸;在吸收脂肪酸的过程中CD36需要发生去棕榈酰化才能进行内吞,从而往细胞内转运脂肪酸。如果阻止CD36的内吞,则能够阻断CD36介导的脂肪细胞中脂肪酸吸收和脂滴的生长。研究人员解析了CD36内吞的信号通路,鉴定了包括LYN,DHHC5,APT1和SYK等参与这一过程的重要分子(图2)。
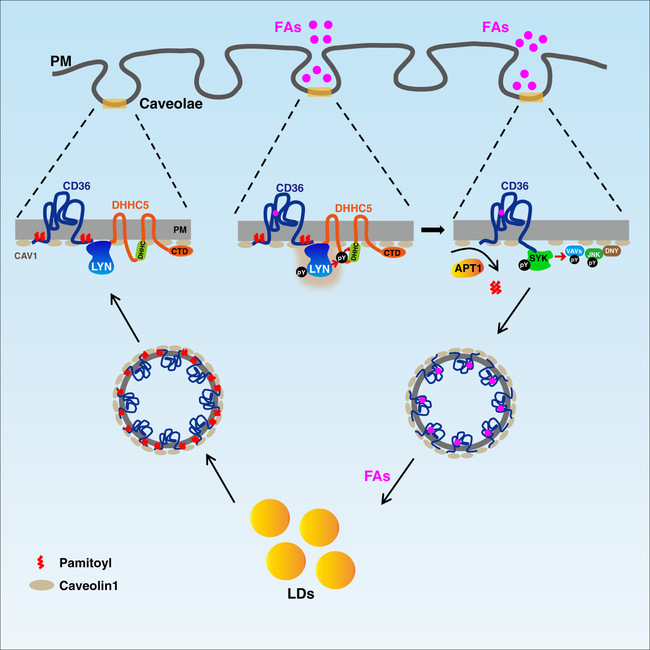
图2 CD36介导的小泡内吞作用促进脂肪酸吸收的工作模型
总的来说,该研究成果揭示了一种新的脂肪酸吸收方式,并且阐明了棕榈酸作为一种脂肪酸的用于修饰CD36反过来调控脂肪酸吸收的分子机制。
据悉,厦门大学生命科学学院的博生生郝建伟、王娟及助理教授郭慧玲为该论文的共同第一作者,复旦大学代谢与整合生物学研究院的赵同金教授与南京大学模式动物研究所的陈帅教授为该论文的通讯作者。同时,该课题获得了包括厦门大学王洪睿教授课题组和云南大学梁斌教授课题组的大力支持。
论文链接:
https://www.nature.com/articles/s41467-020-18565-8
参考文献:
Pepino, M. Y., Kuda, O., Samovski, D. & Abumrad, N. A. Structure-function of CD36 and importance of fatty acid signal transduction in fat metabolism. Annu. Rev. Nutr. 34, 281–303 (2014).
Coburn, C. T. et al. Defective uptake and utilization of long chain fatty acids in muscle and adipose tissues of CD36 knockout mice. J. Biol. Chem. 275, 32523–32529 (2000).
Ring, A., Le Lay, S., Pohl, J., Verkade, P. & Stremmel, W. Caveolin-1 is required for fatty acid translocase (FAT/CD36) localization and function at the plasma membrane of mouse embryonic fibroblasts. Biochim. Biophys. Acta 1761, 416–423 (2006).
Wang, J. et al. DHHC4 and DHHC5 facilitate fatty acid uptake by palmitoylating and targeting CD36 to the plasma membrane. Cell Rep. 26, 209–221.e205 (2019).




 复旦大学网上办事服务大厅
复旦大学网上办事服务大厅 复旦大学实验室安全教育与管理平台
复旦大学实验室安全教育与管理平台