
近年来,免疫治疗革新了癌症的治疗范式,该疗法可通过激活免疫系统清除肿瘤从而获得持久的临床效应。然而现有的免疫疗法如免疫检查点抑制剂(ICBs)的响应率较低,且大部分响应的病人也最终产生耐药而复发,其主要原因是肿瘤免疫抑制微环境和免疫逃逸的存在。在肿瘤微环境中,癌症干细胞(CSC)的存在是肿瘤免疫逃逸、耐药及复发的关键因素,CSC可与免疫细胞(例如依赖于微环境的代谢程序)进而干扰免疫细胞的活性。在肿瘤微环境中的各种免疫细胞中,调节性T细胞(Treg)被认为是介导肿瘤免疫抑制的关键免疫亚群。肿瘤内Treg细胞的积累与患者生存率降低以及肿瘤免疫治疗耐药相关。此外,Tregs可通过多种机制发挥免疫抑制作用,确定影响Treg细胞稳态和功能的因素对于理解癌症发病机制和寻找治疗靶点至关重要。值得注意的是,深入探究CSC与Treg群体之间的相互作用,积极寻找新靶点新药物有望提高肿瘤免疫治疗的效果。
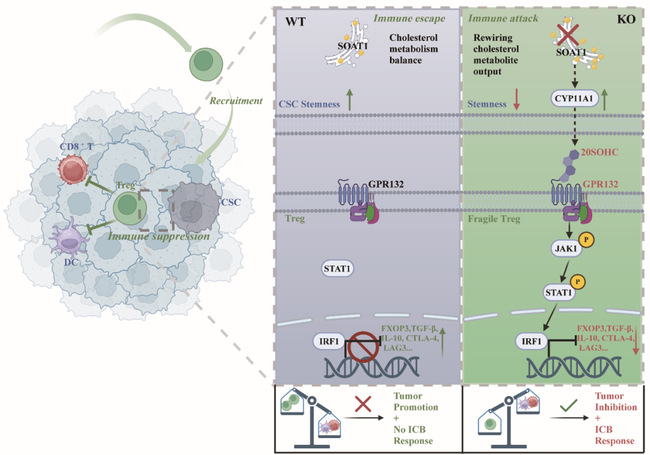
2026年3月17日,复旦大学生命科学学院/代谢与整合生物学研究院侯宪玉团队在Nature Communications杂志上发表了题为“Inhibition of the cancer stem cell immune checkpoint SOAT1 suppresses regulatory T cell functions through a trans-cellular 20(S)-Hydroxycholesterol-GPR132 pathway in mice”的研究论文。该研究首次揭示了胆固醇酯化的关键限速酶SOAT1选择性高表达在CSC中,可促进肿瘤细胞免疫逃逸。利用体内高通量筛选,团队鉴定出新型低毒SOAT1抑制剂STK,并在结肠癌、肝癌、肺癌、黑色素瘤、乳腺癌等多种小鼠模型中激活抗肿瘤免疫反应。机制上,SOAT1抑制可诱导肿瘤细胞释放20(S)-羟基胆固醇(20S-hydroxycholesterol,20S-OHC),20S-OHC激活Treg细胞中的GPR132-JAK1-STAT1-IRF1信号轴,进而重塑GPR132+ Treg细胞亚群,从而增强树突细胞DC的抗原呈递和CD8+ T效应细胞的杀伤功能,使“冷瘤”变成“热瘤”,激活强大的抗肿瘤免疫反应。此外,新型SOAT1抑制剂STK协同增强PD-1抗体、CTLA-4抗体等ICB疗法的疗效。因此,SOAT1作为肿瘤干细胞特异性的代谢免疫检查点可为肿瘤免疫治疗提供新策略,具有重要的理论与实践意义。

一、体内高通量筛选锁定新型SOAT1抑制剂STK
利用RasV12突变的果蝇肾干细胞肿瘤模型和NotchDN突变的果蝇肠干细胞肿瘤模型,研究人员建立了肿瘤免疫治疗候选药物的高通量体内筛选平台,并从6个化合物库的9896个小分子中最终筛选出新型低毒候选化合物STK773477(简称STK),STK能够减弱癌症干细胞干性维持,但对正常干细胞影响较小。通过反向虚拟筛选、药物亲和响应靶标稳定性分析(DARTS)、分子对接分子、等温滴定量热分析、RNA干扰验证及胆固醇代谢验证分析,团队鉴定出SOAT1是STK的作用靶标。
二、代谢检查点SOAT1抑制重塑免疫微环境CSC-Treg细胞间“对话”
研究团队证实SOAT1与CSC标志物CD133等共定位,且SOAT1高表达的肿瘤干细胞具有更强的成瘤能力。这些结果提示,SOAT1是CSC中的关键代谢免疫检查点。新型特异的SOAT1抑制剂STK,在肝癌、肺癌、结肠癌、乳腺癌、黑色素瘤等多种小鼠肿瘤模型中表现出显著的抗肿瘤免疫效应,功能验证实验证实CSC代谢检查点SOAT1抑制依赖Treg细胞发挥抗肿瘤效应。通过对单细胞测序数据的分析,研究团队发现STK治疗后,Treg细胞中一个名为G蛋白偶联受体132(Gpr132)的基因表达显著上调,且在Treg细胞中特异性敲除Gpr132的小鼠中,STK的抑瘤效果明显减弱,这表明GPR132是代谢检查点SOAT1抑制调控Treg功能的核心枢纽。
为了寻找连接代谢检查点SOAT1抑制CSC与GPR132激活(Treg)的桥梁,研究团队通过Bulk RNA-Seq和靶向代谢组学分析,发现STK处理或SOAT1敲低会显著上调肿瘤细胞内氧化胆固醇酶Cyp11a1的表达,并促使肿瘤细胞释放20(S)-羟基胆固醇——(20SOHC)。进一步研究发现,20SOHC能够直接与GPR132结合,进而通过GPR132-JAK1-STAT1-IRF1信号轴调控下游转录因子FXOP3的水平,进一步减少CTLA-4、TGF-β、IL-10等免疫抑制受体的表达和免疫抑制因子的分泌,从而解除Treg细胞的免疫抑制,增加cDC1的抗原呈递和CD8+ T细胞毒性功能,最终重塑免疫激活微环境,增强ICB的协调治疗效应。这一系列发现揭示了一条全新的CSC-Treg细胞间交叉对话通路:肿瘤干细胞SOAT1抑制→肿瘤细胞释放20SOHC → 20SOHC激活Treg细胞GPR132 →启动JAK1-STAT1信号→ Treg功能被抑制→抗肿瘤免疫被“解锁”。
复旦大学生命科学学院丁亚慧博士、方婉琪博士,复旦大学化学院向睿卿硕士和复旦大学生命科学学院刘海涛博士为本文共同第一作者,复旦大学生命科学学院/代谢与整合生物学研究院侯宪玉教授,复旦大学生命科学学院王月桐青年副研究员、孙璘教授和复旦大学化学院凌云教授为本文的共同通讯作者。同济大学附属上海市肺科医院沈莹冉医师,复旦大学生命科学学院周兆才教授,中国科学院昆明动物研究所王国昊研究员及重庆医科大学党永军教授,复旦大学生命科学学院硕士生黄梦林、陈颖博士、硕士生李乔明等在本研究中提供了大力帮助。
原文链接:https://www.nature.com/articles/s41467-026-69305-3
参考文献:
Ding, Y., Fang, W., Xiang, R. et al. Inhibition of the cancer stem cell immune checkpoint SOAT1 suppresses regulatory T cell functions through a trans-cellular 20(S)-Hydroxycholesterol-GPR132 pathway in mice. Nat. Commun[J],(2026).
Tay, C., Tanaka, A. & Sakaguchi, S. Tumor-infiltrating regulatory T cells as targets of cancer immunotherapy. Cancer Cell[J], 2023, 41, 450–465.
Yan, C. et al. Exhaustion-associated cholesterol deficiency dampens the cytotoxic arm of antitumor immunity. Cancer Cell[J], 2023, 41, 1276–1293.e1211.
Lim, S. A. et al. Lipid signalling enforces functional specialization of Treg cells in tumours. Nature[J],2021, 591, 306–311.




 复旦大学网上办事服务大厅
复旦大学网上办事服务大厅 复旦大学实验室安全教育与管理平台
复旦大学实验室安全教育与管理平台