
基因组“暗物质”涵盖了启动子、增强子等非编码调控元件,占据人类基因组约98%的序列。起初被误认为是“垃圾DNA”;而随着人类基因组计划兴起,明确这些暗物质在基因表达调控中的作用。尽管基因组关联性研究成功识别大量与复杂疾病相关的非编码位点【1,2】,但这些候选位点的致病性仍面临双重挑战,如由于连锁不平衡效应,这些位点大多作为标签SNPs难以锁定具有生物学功能的精确位点;缺乏经典孟德尔共分离的遗传学证据,如经亲本配子往子代的垂直跨代传递。由于很难建立与疾病发生的直接因果关系,与临床转化依然存在较大的“GAP”。如何界定“暗物质”的功能边界并打通从遗传发现到临床诊断的转化路径,已成为当前遗传研究中精准医学领域亟待突破的关键问题。当前全球范围内基于人群家系连锁分析的非编码突变的致病性研究还鲜有报道。
相比于严重影响生殖健康和配子传递效率的结构性畸形如先心病,感官缺陷(如近视)人群为解析非编码区的跨代遗传机制提供理想模型。当前我国的高度近视人群数以亿计,已成为导致视力损伤及致盲的首要眼病之一;其中,眼轴长度的异常增长是高度近视的核心表型,也是开展早期预防与远期并发症管理的关键切入点。尽管多个与近视相关的易感基因座(Loci)已被识别,目前大部分基因座背后真实的致病因子依然处于‘黑箱’状态,亟待深入挖掘。
2026年4月1日,复旦大学附属妇产科医院/代谢与整合生物学研究院王红艳教授、复旦大学附属妇产科医院周翔宇研究员与复旦大学附属眼耳鼻喉医院于志强主任联合在Cell Research发表名为“Increased PRSS56 expression is a causal factor and therapeutic target for human axial high myopia”的研究论文,揭示PRSS56基因非编码区突变作为独立风险因子导致轴性高度近视的分子机理,并发现PRSS56高表达是近视发生的潜在生物标记物;基于PRSS56的光响应特性,团队在动物模型中开发蓝光照射干预策略,为户外暴露利于青少年近视防控提供相关的理论支撑。

团队对两个来自中国南北方的遗传性高度近视大家系(常染色体显性)进行连锁单倍型分析,将位点定位于2q37.1一个3.9Mb区段,该区段曾被国外学者报道与遗传近视密切相关,但一直未找到具体致病因子【3】。团队起初通过基因组芯片和高深度外显子测序在该区段没有发现符合共分离原则的位点,通过全基因测序(WGS)分析发现PRSS56基因翻译起始上游c.-187G>T和c.-187G>C是区段内唯一符合筛查标准的遗传位点,且在所有17名患者中共分离,在GnomAD数据库(0/152,330)和653例对照组均无检出。在散发儿童早发病例中亦检出PRSS56其他多个启动子变异位点,并在36个具有高等视觉物种中高度保守,提示PRSS56调控区为高度近视发生的热点基因座。
在细胞层面,团队先后利用:1)患者来源iPSC细胞、2) iPSC诱导分化的视网膜类器官、3)RPE细胞双荧光素酶证实该非编码变异通过增强EGR1结合促进自身基因表达。
在动物模型层面,团队先后构建拟人化的PRSS56点突变敲入KI模型、基因敲除KO、AAV腺病毒注射、Tet-on视网膜诱导等4个转基因模型证明PRSS56以剂量与酶活依赖的方式决定眼轴长度;PRSS56表达升高导致小鼠屈光度向近视方向偏移及视网膜巩膜变薄。PRSS56上调伴随巩膜Myosin-4水平下降及I型胶原减少,提示其通过巩膜重塑参与轴性延长过程。
团队发现由形觉剥夺和透镜诱导的豚鼠近视模型均出现Prss56基因高表达趋势,短波蓝光辐照可通过抑制Prss56表达并减缓造模后眼轴进一步增长,提示Prss56是高度近视的生物标志物和潜在的光响应蛋白,成为连接遗传变异与环境因素(如户外运动增加光照暴露)的关键纽带。
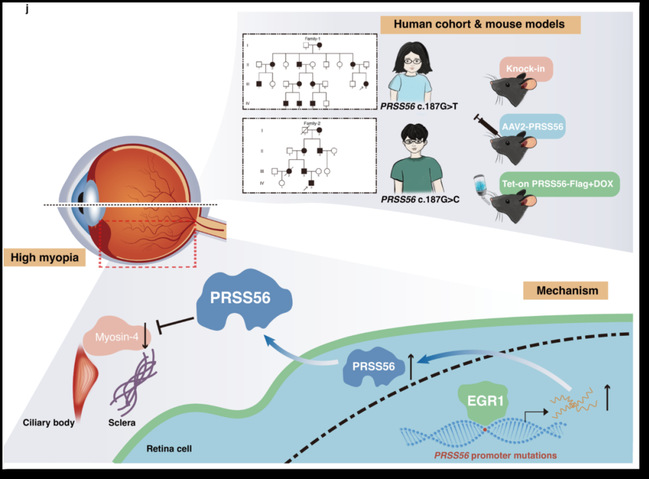
图一:PRSS56基因非编码突变致病机理的系统解析
已有报道PRSS56基因编码区丧失功能性突变导致小眼畸形并伴发远视【4】,本研究提出“表达增益型”模式对阐述PRSS56在眼球发育中的角色提供反向支撑,并解析PRSS56作为一个丝氨酸胰蛋白酶在眼球发育调控中的催化底物。根据动物模型数据,团队发现即使错过视力发育的关键窗口期,PRSS56高表达依然可以实现巩膜重塑来调控眼轴的伸长,体现其在近视防控和靶点开发中的转化潜力,为儿童与青少年高度近视的精准干预开辟新方向。
随着最新基因解码工具 AlphaGenome 的问世,人类对于基因组“暗物质”的分析与认知即将迎来重大突破【5】。
复旦大学代谢与整合生物学研究院吴帛轩博士(已毕业),复旦大学曾炜佳博士(已毕业)、汤柯夫博士后(已出站)、熊佳伟博士(已毕业)为本文的共同第一作者。复旦大学附属妇产科医院/代谢与整合生物学研究院王红艳教授、复旦大学附属妇产科医院周翔宇研究员、复旦大学附属眼耳鼻喉医院于志强主任医师为本文的共同通讯作者。
原文链接:https://www.nature.com/articles/s41422-026-01241-9
参考文献:
Genomic analyses implicate noncoding de novo variants in congenital heart disease. Nat Genet. 2020;52(8):769-777.
Genome-wide meta-analyses of multiancestry cohorts identify multiple new susceptibility loci for refractive error and myopia. Nat Genet. 2013;45(3):314-8.
Identification of a novel locus on 2q for autosomal dominant high-grade myopia. Invest Ophthalmol Vis Sci. 2005;46(7):2300-7.
Alteration of the serine protease PRSS56 causes angle-closure glaucoma in mice and posterior microphthalmia in humans and mice. Nat Genet. 2011;43(6):579-84.
Advancing regulatory variant effect prediction with AlphaGenome. Nature. 2026;649(8099):1206-1218.




 复旦大学网上办事服务大厅
复旦大学网上办事服务大厅 复旦大学实验室安全教育与管理平台
复旦大学实验室安全教育与管理平台