
复杂生物体的胚胎发育,依赖于持续而精确的营养供给【1,2】。对于卵生动物而言,这些营养在受精前就已储存在卵黄之中。因此,卵黄是胚胎早期发育的“营养仓库”,是研究营养利用调控机制的理想模型【3,4】。长期以来,人们普遍认为卵黄中的营养会随着发育进程逐渐被消耗。然而,不同类型的营养是否以相同的节奏被利用,以及它们如何受到发育程序的调控,这些问题一直缺乏清晰的认识。
2026年4月,复旦大学代谢与整合生物学研究院戴薇课题组在Cell Reports上发表题为“Increased Yolk Lipid Mobilization Promotes Zebrafish Post-Segmentation Growth via an Hnf4-Lipoprotein Axis”的研究论文,系统比较了斑马鱼卵黄中蛋白质与脂质这两类主要营养物质的动员规律。研究发现,卵黄中的蛋白质持续被降解,而脂质并非从一开始就被大量使用,而是在体节形成之后才显著加速消耗。这一过程依赖于受精后激活的Hnf4a/b转录因子。该转录因子启动卵黄中的脂蛋白装配与运输程序,将脂质输送到胚胎体内,从而支持后期快速生长。这项研究揭示了由Hnf4–脂蛋白轴介导的母源脂质“阶段性动员”新机制。

研究人员首先定量分析了斑马鱼卵黄中蛋白质与脂质的含量。结果发现,两种营养的变化模式并不同步:蛋白质含量持续减少,而脂质在胚胎发育前期(0-24小时)消耗有限,却在后期(24-48小时)明显加速。斑马鱼的卵黄营养主要储存在类似溶酶体的卵黄颗粒中,而卵黄外层的卵黄合胞层(YSL)则充当代谢中枢。通过解剖分离卵黄并进行转录组分析,研究人员发现,YSL中溶酶体相关基因高度富集,其中蛋白降解基因多在前期高表达,而脂质降解与转运基因则在后期被激活。
研究人员进一步比较了干扰卵黄蛋白与脂质利用对胚胎发育的影响。由于卵黄中表达多个组织蛋白酶基因,且其中许多为母源表达,研究者使用组织蛋白酶抑制剂E64D来阻断卵黄蛋白的降解。结果显示,胚胎发育至24小时已出现明显体轴缩短,神经与肌肉发育受损,而补充游离氨基酸可部分挽救这些缺陷。另一方面,为了干扰卵黄脂质的动员,研究者鉴定出两种定位于卵黄颗粒的酸性脂肪酶——Pla2g15和Lipf。敲除pla2g15导致更多磷脂残留在卵黄中,而敲除lipf则引起中性脂质积累增加。这些突变体同样在24小时时基本正常,到48小时才出现生长缺陷。经Pla2g15和Lipf降解后的卵黄脂质,需要在卵黄合胞层(YSL)中重新包装成脂蛋白,再通过循环系统输送至全身。当负责脂蛋白装配的Mttp缺失时,胚胎在24小时仍接近正常,但到48小时出现明显的生长迟缓。这表明,胚胎发育过程中,蛋白降解更像一个持续的基础过程,脂质动员则具有明确的后期增强特征。
那么,卵黄脂质的利用是如何被激活的?通过分析脂质动员相关基因启动子区域,研究者锁定了卵黄特异表达的转录因子Hnf4。斑马鱼中存在两个同源基因,即hnf4a和hnf4b,其双突变胚胎在24小时前基本正常,到48小时时则出现明显生长迟缓。转录组分析显示,在双突变体中,脂质降解和脂蛋白组装与运输相关基因的表达显著下调。在YSL中回补hnf4a mRNA后,相关基因表达得以恢复,生长缺陷也得到挽救。这一结果证实,Hnf4a/b是启动卵黄脂质动员的关键开关。
最后,研究人员分析了小鼠和人类卵黄囊的公开数据,发现其中同样富集HNF4、MTTP及多种脂蛋白相关基因。这一结果提示,以HNF4为核心的脂蛋白表达程序,可能在脊椎动物的卵黄囊中相对保守。
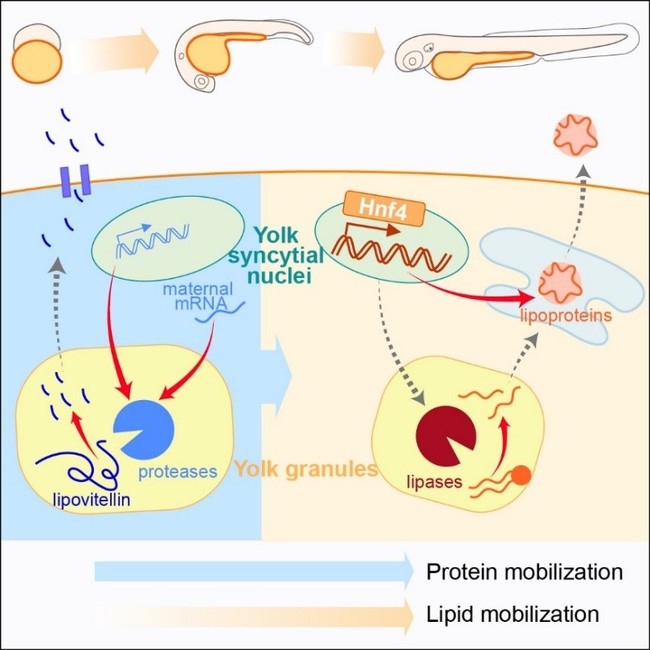
图:斑马鱼胚胎发育过程中卵黄蛋白质和脂质动员模式图
本研究揭示了斑马鱼卵黄中母源蛋白与脂质存在不同的时序调控模式,并阐明了由Hnf4—脂蛋白轴介导的母源脂质“阶段性动员”新机制。这项工作不仅深化了对卵黄利用机制的理解,也为认识脊椎动物早期发育中的营养时序调控提供了新的理论框架。
复旦大学代谢与整合生物学研究院博士研究生孙通、陶怡竹、曾莹洁以及硕士研究生艾冉为本文共同第一作者。复旦大学代谢与整合生物学研究院戴薇、陈立准聘副教授和复旦大学脑科学转化研究院倪金飞副教授为本文共同通讯作者。上海交通大学附属仁济医院陈磊研究员和复旦大学代谢与整合生物学研究院黄林章准聘副教授为本研究提供了重要帮助与支持。
原文链接:https://doi.org/10.1016/j.celrep.2026.117295
参考文献:
1.Solmonson, A., Faubert, B., Gu, W., Rao, A., Cowdin, M.A., MenendezMontes, I., Kelekar, S., Rogers, T.J., Pan, C., Guevara, G., et al. (2022). Compartmentalized metabolism supports midgestation mammalian development. Nature 604, 349–353.
2.Aye, I.L.M.H., Aiken, C.E., Charnock-Jones, D.S., and Smith, G.C.S. (2022). Placental energy metabolism in health and disease-significance of development and implications for preeclampsia. Am. J. Obstet. Gynecol. 226, S928–S944.
3.Ramos, I., Machado, E., Masuda, H., and Gomes, F. (2022). Open questions on the functional biology of the yolk granules during embryo development. Mol. Reprod. Dev. 89, 86–94.
4.Riddle, M.R., and Hu, C.K. (2021). Fish models for investigating nutritional regulation of embryonic development. Dev. Biol. 476, 101–111.




 复旦大学网上办事服务大厅
复旦大学网上办事服务大厅 复旦大学实验室安全教育与管理平台
复旦大学实验室安全教育与管理平台